
住友制药在开展临床试验时,遵循《赫尔辛基宣言》,《人用药品注册技术要求国际协调会议药物临床试验质量管理规范(ICH-GCP)》以及相关国家的法律、法规和准则。在临床试验开始前获得药监部门的许可,研究中心的伦理许可和妥善征得受试者的同意。
住友制药根据《赫尔辛基宣言》、《药物临床试验质量管理规范(Good Clinical Practice, GCP)》个人信息保护法和所有相关法律法规进行临床试验。充分考虑保护临床试验受试者人权及个人信息和隐私。住友制药还通过妥善管理临床试验数据,以确保临床试验受试者的个人信息和隐私。
住友制药拥有全球质量保证体系,在临床试验中遵守各项标准操作程序(SOP和SWI)。对临床试验进行定期的监查、质量控制和稽查。及时对员工进行教育和培训。
住友制药遵守所在国的相关法律和法规、人类遗传资源管理条例,有效保护和合理利用人类遗传资源,维护公众健康、国家安全和社会公共利益。
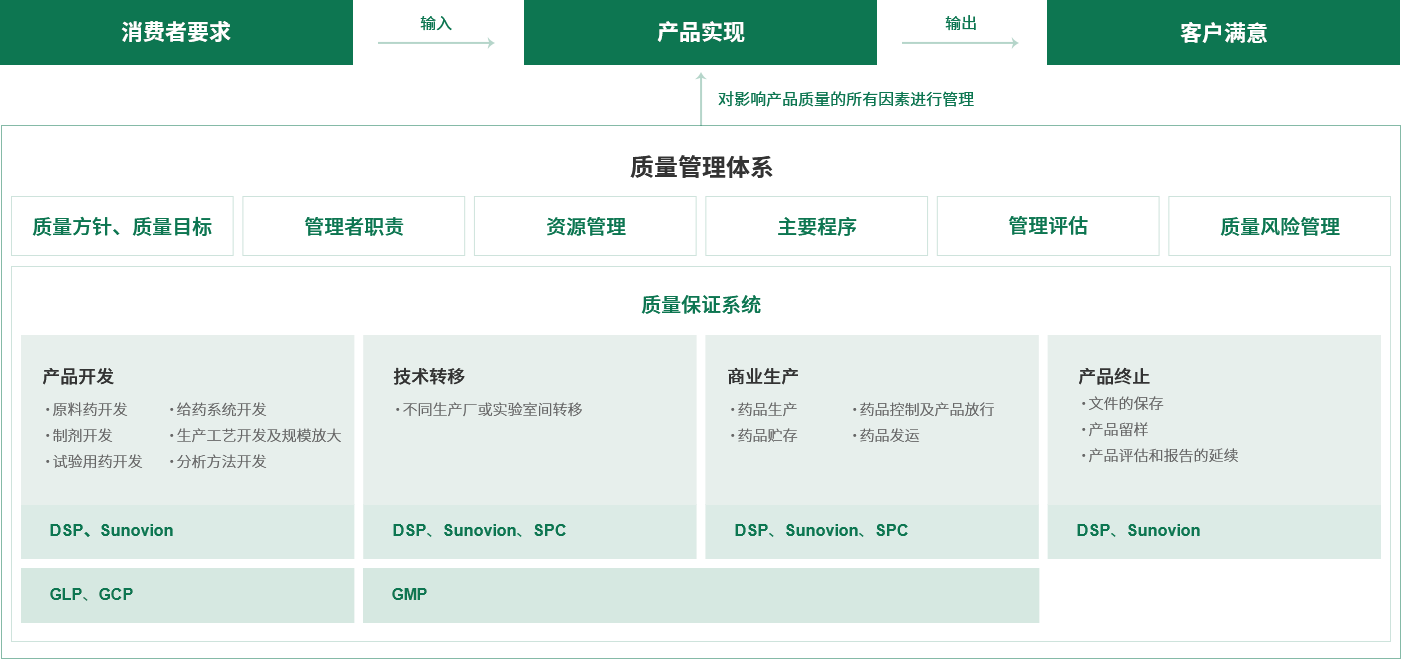
住友制药质量保证的目标是不断提升产品质量和服务质量,持续改进质量管理体系,将药品注册的有关安全、有效和质量可控的所有要求,系统地贯彻到药品生产、控制及产品放行、贮存、发运的全过程中,确保所生产的药品符合预定用途和注册要求,为人类健康事业奉献优质高效的药品。

作为住友制药在中国的全资子公司以及海外药品上市许可持有人的境内代理机构,是全球药物警戒体系的重要组成部分。
住友制药为科学实施对药品全生命周期的管理和监测,落实中国国家法律法规及地方法规和指南的要求,担负企业作为药品安全责任人的责任和义务,通过近十年的发展,我们建立了各项药物警戒管理制度,与总公司和相关产品的境外持有人的药物警戒及相关部门共同组成了完整的、系统的、有效的药物警戒体系,从而为中国患者合理用药、安全用药提供技术支撑和科学保障。
我们使终把患者安全放在首位,践行以“患者为中心”的经营理念,履行相关的责任和义务。

您即将离开住友制药官网,并跳转至第三方网站,请注意相关风险。